医薬品工場
クオリフィケーション対応
ISPE Baseline®Pharmaceutical Engineering Guide Volume 5(Commissioning & Qualification)やPIC/S GMP Annex15(Qualification & Validation)などのレギュレーションやガイドラインに準じて、査察をスムーズに対応できる確実かつ効率的なクオリフィケーションをリスクベースで実施します。
ユーザー要求(UR)・ユーザー要求仕様書(URS)・クオリフィケーションマスタープラン(QMP)作成からクオリフィケーションマスターレポート(QMR)作成までお客様と共に、シミズが主体となって一貫したクオリフィケーションを実施することが可能です。
クオリフィケーションフロー
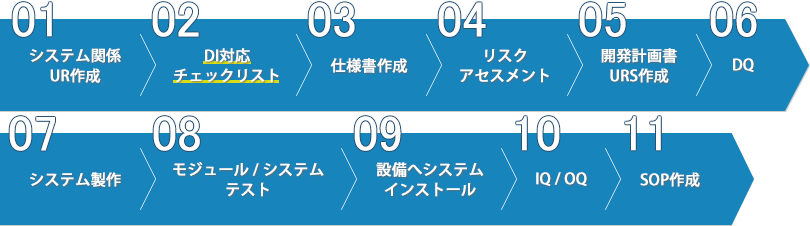
クオリフィケーション業務は以下のフローチャートに従って、運営していきます。
欧米では昨今クオリフィケーションの起点となるURSの内容を査察にて確認するケースが増えております。シミズではURS作成前にリスクアセスメントを実施し、その結果をURSへ反映、さらにトレサビリティマトリクスにて各URS項目が設計・検証項目に確実に反映されていることを管理します。

リスクアセスメント
基本設計および詳細設計段階にICH Q9やISPE GAMP5に基づいて、品質リスクアセスメントを実施し、施設・設備などに潜在するリスクを顕在化する事で、リスクのレベルに対して適切に対処します。これにより効率的かつリスクベースの設計・クオリフィケーション業務を実現します。
■リスクアセスメントの内容
- システムインパクトアセスメント
プロジェクトにて導入する全システムのリストを作成し、ISPE Baseline®Pharmaceutical Engineering Guide Volume 5(Commissioning & Qualification)の基準に則り、クオリフィケーション対象の絞り込みを行います。 - CSV(コンピュータ化システムバリデーション)関連リスクアセスメント
CSV関連のリスクアセスメントに関しては21 CFR Part11やISPE GAMP5に基づいて以下の評価を実施し、URにて意図したシステムが確実に構築・検証されることを確認します。
- サプライヤ監査:システム供給サプライヤの実績・社内QMSの評価を行います。
- カテゴリー分類評価:導入するシステムのハード・ソフトの構成・仕様を確認し、CSVカテゴリーを決定します。
- ER/ES(電子記録/電子署名)確認:電子記録/電子署名に関する要求事項とそれに対するシステムの対応状況を確認します。
- 機能的リスクアセスメント
お客様・シミズ・必要に応じてベンダーのSME(Subject Matter Expert)より構成されたリスクアセスメントチームにより、各システムに対してブレインストーミング型のリスクアセスメントを実施します。リスクアセスメントにて顕在化したリスクに関しては定量化を図って評価を行い、許容できないリスクに対しては対応策を講じます。
リスクアセスメントの結果をURSへ反映させて、その結果を起点としてリスクベースのクオリフィケーションを展開していきます。
トレサビリティマトリクス
リスクアセスメントの結果を反映させたURSの各要求項目がどのように設計へ反映され、その結果をどのように検証したのかを管理するためにトレサビリティマトリクスを採用します。
トレサビリティマトリクスは医薬品業界ではISPE GAMPガイドで提唱されておりますが、シミズではコンピュータ化システムの要求項目だけでなく、全ての要求項目を対象とし、 DQ・FAT・IQ・OQにて漏れなく確実に検証されていることを管理していきます。
データインテグリティ対応
昨今医薬品業界では「データインテグリティ(DI)」が大きな話題となり、その対応を強く求められています。
「DI」への対応としては全てシステム化し、セキュリティ対応・監査証跡・データの改ざん防止などに対応できることが望ましいですが、導入に大きなコストもかかるため、システムと運用のコンビネーションで対応することも検討する必要があります。
シミズでは下記のフローチャートにて、お客様のデータインテグリティ対応をサポートします。
■DI対応フローチャート
特に設計段階で「DI対応チェックリスト」にてUR要件の対応状況の見える化を行うことで、運用でカバーする項目を明確にし、その後の確実な機能の検証とSOPへの落とし込みをサポートします。
■DI対応チェックリスト
以下の項目に対して、URにて要求するシステムがどこまで対応できているかを見える化し、対応していない項目に対して運用でどのようにカバーするかを検討します。
| DIチェックリスト(例) | |||||
|---|---|---|---|---|---|
| システム | 対応項目 | 対応の可否 | 対応方法 | 評価 | 確認 |
| セキュリティ | ログイン(ユーザーID&パスワード) | ||||
| アクセス制限 | |||||
| パスワード有効期限 | |||||
| ユーザーIDの有効/無効化 | |||||
| 自動ログオフ ・・・etc. | |||||
| 電子記録 | 改ざん防止 | ||||
| データの同時性 | |||||
| データのバックアップ/復元性 | |||||
| データの誤入力防止 | |||||
| 時刻の動き | |||||
| 監査証跡 ・・・etc. | |||||
| 電子署名etc. | 本人特定 (ユーザーID&パスワード、バイオメトリクス認証) |
||||
| 権限管理 | |||||
| 偽造対応 ・・・etc. | |||||